IMDRF-Codes: Der Schlüssel zur standardisierten Datenverwaltung in der Medizintechnik
Als international standardisiertes System sorgen die IMDRF Codes für eine klare Kommunikation zwischen Medizinprodukteherstellern und Regulierungsbehörden. Sie schaffen die Grundlage für Transparenz und Zusammenarbeit auf globaler Ebene.
Doch wie genau sind diese Codes aufgebaut? Welche Inhalte verbergen sich dahinter? Und vor allem: Wie und wo können diese Codes in der Praxis anwendet werden? In diesem Blogbeitrag nehmen wir die IMDRF-Codes genauer unter die Lupe, erklären ihre Anwendung und geben Ihnen wertvolle Tipps, die Ihnen die Anwendung erleichtern.
Als besonderes Highlight möchten wir Ihnen unsere benutzerfreundliche Web-Applikation vorstellen, die den Umgang mit den IMDRF-Tabellen deutlich vereinfacht und für mehr Übersichtlichkeit sorgt. Per Mausklick können die relevanten Codes gesammelt und anschließend zusammen in Ihr System übernommen werden. So wird die Arbeit nicht nur einfacher, sondern auch deutlich effizienter. Wir zeigen Ihnen, wie Sie diese Applikation optimal nutzen können. Doch zunächst geht es in diesem Beitrag um die Grundlagen der IMDRF-Codes.
Was ist IMDRF?
Das IMDRF steht für International Medical Device Regulators Forum und ist der Nachfolger der Global Harmonization Task Force (GHTF).
Das IMDRF ist eine freiwillige Gruppe von Regulierungsbehörden für Medizinprodukte aus der ganzen Welt, die sich mit dem Ziel zusammengeschlossen haben, um eine internationale Annäherung und Harmonisierung der Vorschriften für Medizinprodukte zu erreichen. Das IMDRF ist in Arbeitsgruppen organisiert, die sich mit verschiedenen Themen befassen und dazu Dokumente veröffentlichen.
Mitglieder sind derzeit Australien, Brasilien, Kanada, China, die Europäische Union, Japan, Russland, Singapur, Südkorea, das Vereinigtes Königreich und die USA.
Weitere Informationen finden Sie auf der offiziellen Homepage der IMDRF IMDRF.
IMDRF Codes – Meldung von unerwünschten Vorkommnissen (Adverse Event Reporting – AER)
Ziel der IMDRF Adverse Event Terminology Working Group ist die Entwicklung und Förderung einer harmonisierten Terminologie und eines standardisierten Systems zur Beschreibung von Informationen über Vorkommnisse und Zusammenhänge von Medizinprodukten.
Dieses System besteht aus alphanumerischen Codes, die in erster Linie für Medizinproduktehersteller (Berichterstatter) und Regulierungsbehörden entwickelt wurden, um die Meldung von unerwünschten Vorkommnissen zu erleichtern.
Warum können IMDRF Codes helfen?
Tritt mit einem sich auf dem Markt befindlichen Medizinprodukt ein unerwünschter Vorfall auf, muss dieser nach verschiedenen Vorschriften gemeldet werden. Die Beschreibungen des Vorkommnisses enthalten in der Regel viel Text, der beschreibt, was passiert ist, wie ein Produkt an dem Vorkommnis beteiligt war, welche Auswirkungen das Vorkommnis auf den Patienten, Anwender oder Dritte hatte, welche Maßnahmen ggf. bereits ergriffen wurden, etc. Dabei führen je nach Autor unterschiedliche Begriffe, Formulierungen und Erläuterungen des Sachverhalts dazu, dass gemeldete Vorkommnisse nicht unmittelbar miteinander verglichen und damit für Analysen verwendet werden können.
Um diese meist umfangreichen Beschreibungen zusammenzufassen und zu vereinheitlichen, werden einzelne Textbausteine in IMDRF Codes umgewandelt. Das hat folgenden Vorteile:
- Kurze und präzise Erfassung und Meldung von Vorkommnissen im Zusammenhang mit Medizinprodukten
- Reduktion von Mehrdeutigkeiten und damit die Steigerung der Effizienz des Bewertungsprozesses
- Nutzung zur Identifizierung potentieller neuer Risiken und zu Trendanalysen, was eine schnellere Reaktion der Regulierungsbehörden und Hersteller ermöglicht.
- Nutzung von Datenbanken oder anderen elektronischen Systemen durch die Regulierungsbehörden zur Überwachung und Analyse unerwünschter Vorkommnisse und damit zur Verbesserung des Schutzes von Patienten und der öffentlichen Gesundheit.
Einsatzbereiche der IMDRF Codes: Ein Überblick
Die Codes des International Medical Device Regulators Forum (IMDRF) sind ein wesentliches Instrument für die standardisierte Kommunikation im Bereich der Medizinprodukte. Sie dienen nicht nur der effizienten Kommunikation zwischen Herstellern und Regulierungsbehörden, sondern werden in verschiedenen Bereichen des Lebenszyklus von Medizinprodukten eingesetzt. Die wichtigsten Anwendungsbereiche sind:
Kommunikation mit Regulierungsbehörden
Ein wichtiges Anwendungsgebiet der IMDRF Codes ist die Berichterstattung an Regulierungsbehörden. Sie werden im Manufacturer Incident Report (MIR) (DocsRoom – European Commission) für schwerwiegende Vorkommnisse und Zwischenfälle angegeben. Innerhalb dieses Formulars werden sie benötigt, um spezifische Informationen über Probleme mit Medizinprodukten anzugeben (Abschnitt „3.2 Medical device problem information“). Außerdem helfen sie dabei, ähnliche Vorkommnisse zu identifizieren und zu gruppieren (Abschnitt „4.3.1 Use of IMDRF terms and codes for identifying similar incidents“). Dies fördert eine klare und einheitliche Darstellung der Vorkommnisse und erleichtert die Analyse.
Post Market Surveillance (PMS)
Nach der Markteinführung eines Medizinproduktes ist die Überwachung der Produktsicherheit von zentraler Bedeutung. Im Rahmen der Post Market Surveillance (PMS) spielt auch die Nutzung der IMDRF Codes eine Schlüsselrolle. Gemäß der MDCG Guidance 2022-21 (Guidance – MDCG endorsed documents and other guidance – European Commission) sollen diese Codes in den Periodic Safety Update Reports (PSUR) zur konsistenten und nachvollziehbaren Darstellung von Vorkommnismeldungen verwendet werden. Sie ermöglichen damit eine strukturierte Auswertung sicherheitsrelevanter Daten und unterstützen den kontinuierlichen Verbesserungsprozess von Medizinprodukten.
Interne Nutzung: Trendanalysen und Qualitätsmanagement
Die Codes der Hersteller können auch intern effektiv genutzt werden. Sie bieten eine standardisierte Grundlage für Trendanalysen, bei denen wiederkehrende Muster von Problemen oder Vorkommnissen erkannt werden können. Durch die Anwendung der Codes können Auffälligkeiten systematisch kategorisiert und Maßnahmen zur Verbesserung der Produktqualität und -sicherheit ableitet werden
Struktur der IMDRF Codes
Übergeordnete Struktur
Die Struktur der unerwünschten Vorkommnisse besteht aus vier Hauptgruppen:
- Medical Device Problem: Beobachtungen auf der Ebene des Medizinprodukts
- Cause Investigation: Untersuchungen zu möglichen Ursachen des Vorkommnisses und kausalen Zusammenhängen zwischen der Anwendung des Produkts (unabhängig davon, ob es eine Fehlfunktion vorliegt) und gesundheitlichen Beeinträchtigungen
- Health Effects: Beobachtungen auf der Ebene der Probanden, d. h. typischerweise gesundheitliche Beeinträchtigungen bei Patienten, Anwendern oder Dritten
- Component: Beobachtungen an seinen Bestandteilen einschließlich Zubehör
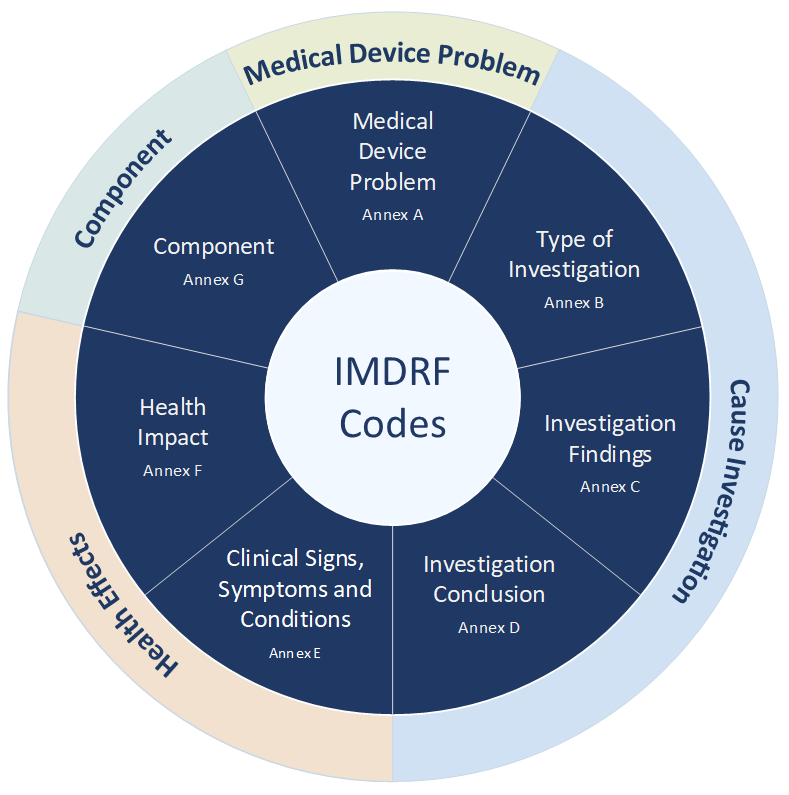
Darüber hinaus gibt es sieben Anhänge die von der Arbeitsgruppe erarbeitet und in vier Hauptgruppen eingeteilt wurden (siehe Abb. 1)
- Annex A: IMDRF terminologies for categorized Adverse Event Reporting (AER) – Medical Device Problem
- Annex B: IMDRF terminologies for categorized Adverse Event Reporting (AER) – Type of Investigation
- Annex C: IMDRF terminologies for categorized Adverse Event Reporting (AER) – Investigation Findings
- Annex D: IMDRF terminologies for categorized Adverse Event Reporting (AER) – Investigation Conclusion
- Annex E: IMDRF terminologies for categorized Adverse Event Reporting (AER) – Health Effects – Clinical Signs and Symptoms or Conditions
- Annex F: IMDRF terminologies for categorized Adverse Event Reporting (AER) – Health Effects – Health Impact
- Annex G: IMDRF terminologies for categorized Adverse Event Reporting (AER) – Medical Device Component
Eine detaillierte Erläuterung und Aufschlüsselung der Anhänge mit zusätzlichen Beispielen findet sich weiter unten im Beitrag (Weitere Erläuterungen zu den Anhängen A-F).
Alternativ können Informationen in dem von der Arbeitsgruppe erstellten Dokument „IMDRF terminologies for categorized Adverse Event Reporting (AER): terms, terminology structure and codes“ im Abschnitt 4.5 Description of the four sets of terminologies Terminologies for Categorized Adverse Event Reporting (AER): terms, terminology and codes | International Medical Device Regulators Forum entnommen werden.
Aufbau und Erläuterung der einzelnen Level
In den genannten Anhängen werden die Codes in einer hierarchischen Codestruktur dargestellt. Allgemeine, übergeordnete Begriffe bilden dabei die Einstiegsebene Level 1. Diese auf Level 2 und Level 3 im Detailgrad zunehmen und den allgemeinen Begriff auf Level 1 genauer beschreiben.
Im Folgenden werden die genannten vier Schlüsselbegriffe (Begriff/Terminologie, Code und hierarchische Kodierungsstruktur) kurz erläutert:
- Begriff/Terminologie: Die Verwendung von Terminologien (d. h. eines kontrollierten Satzes klar definierter Begriffe) kann bei der Beschreibung von Vorkommnissen helfen, indem sie die Mehrdeutigkeit des narrativen Textes durch die Kategorisierung von Vorkommnissen reduziert wird.
- Code/Kodierung: Die Mehrdeutigkeit kann weiter reduziert werden durch die Verwendung von alphanumerischen Codes, die einem vordefinierten Begriff aus einer bestimmten vordefinierten und kontrollierten Terminologie zugeordnet werden. Die Zuweisung dieser Codes wird als „Kodierung“ bezeichnet.
- Unter einer hierarchischen Kodierungsstruktur versteht man die logische Anordnung solcher kodierter Begriffe in mehrstufigen Verzweigungsstrukturen, also vergleichbar mit einem logischen Entscheidungsbaum.
Eine Zeile besteht aus zwei Hauptkomponenten dem Begriff/Terminologie, der in Schriftform als Text dargestellt wird und dem alphanumerischen Code. Durch den Code kann jeder Begriff eindeutig identifiziert werden.
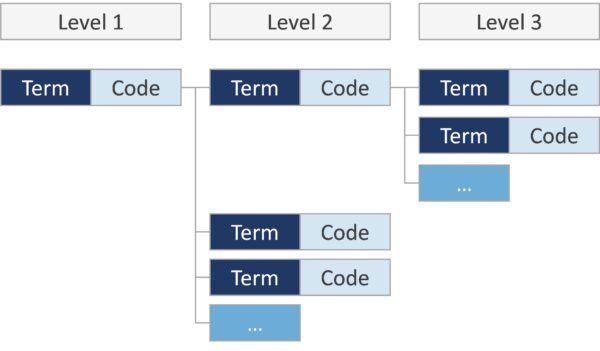
Aufbau und Erläuterung der Codes
Der Aufbau der Codes sieht wie folgt aus:

Ein Code beginnt immer mit einem Großbuchstaben (A–G), der angibt, zu welcher Anlage der Code gehört. Darauf folgt der alphanumerische Code, der aus jeweils zwei Ziffern besteht (nn[nn][nn]). Die Ziffernfolge kann somit aus zwei, vier oder sechs Ziffern bestehen. Die Anzahl der Ziffernpaare geben die Ebene an auf der sich der Code befindet. Je mehr Ziffern ein Code umfasst, desto detaillierter sind die Informationen.
Erläuterung zur Struktur der Tabellen
Wo finde ich die Begriffe und Codes der Anhänge? Die Arbeitsgruppe hat für jeden Anhang A-G eine Tabelle erstellt. Diese Tabellen können als JSON oder XLSX auf der Seite des IMDRFs heruntergeladen werden: Terminologies for Categorized Adverse Event Reporting (AER): terms, terminology and codes | International Medical Device Regulators Forum.
Die Struktur dieser Tabellen werden im Folgenden näher erläutert.
Informationsfeld
Zu Beginn jeder Tabelle gibt es eine Infobox mit den folgenden Inhalten:

- Name des Anhangs
- Titel des Anhangs
- Revision des Dokuments
- Beschreibung des Anhangs
- Informationen zum Einsatz des Anhangs
- Freigabe des Dokuments
Begriffe/Terminologien und Codes
Unterhalb der Infobox sind die Begriffe, wie oben beschrieben, in Level (1-3) unterteilt. Jedem Begriff auf jedem Level wird ein eindeutiger alphanumerischer Code zugeordnet. Ausnahmen bei der Anzahl der Level gibt es in den Anhängen B und D. In Anhang B gibt es ausschließlich das Level 1 und in Anhang D Level 1 und Level 2.
In dem hier aufgeführten Beispiel aus Anhang A ist das Problem des Medizinprodukts ein elektrisches/elektronisches Problem (Level 1). Level 2 gibt an, um welches elektrische Problem es sich handeln könnte, in diesem Beispiel ein Batterieproblem. Auf dem dritten Level (Level 3) wird das Batterieproblem noch detaillierter beschrieben, z.B. Ausfall des Batteriebetriebs (A070503).
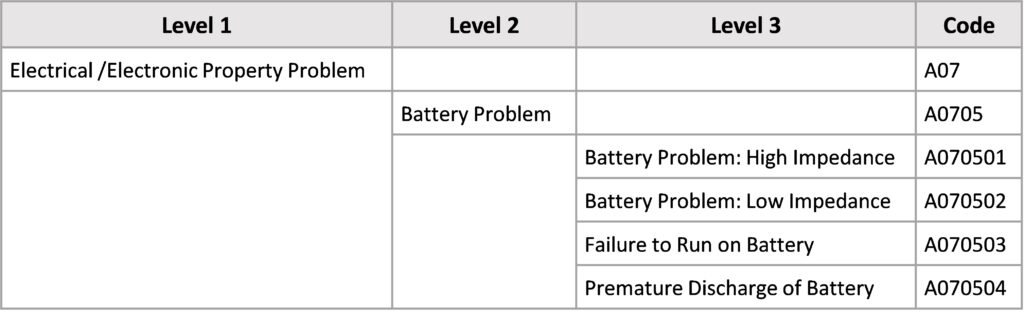
Die hierarchische Struktur zeigt genau um welchen Fall es sich handelt. Allein aus dem Codes sind folgende Informationen ersichtlich:
- Auf welchen Annex bezieht sich der Code (im Beispiel Annex A)
- Auf welches Level bezieht sich der Code – wie detailliert wurde das Vorkommnis beschrieben
Beschreibungen, Definitionen und Beispiele
Zusätzlich werden zu den Begriffen der verschiedenen Level und Codes Definitionen angegeben, um die Begriffe zu erläutern. Nachfolgend ein Beispiel für die Beschreibungen der Codes A01, A0101 und A010101:

In den weiteren Spalten werden zusätzliche Informationen zum Status und zur Historie der einzelnen Begriffe gegeben.
Ein Change Log und die Release Notes zur jeweils aktuellsten Version der Tabellen sind ebenfalls auf der IMDRF Website verfügbar: Terminologies for Categorized Adverse Event Reporting (AER): terms, terminology and codes | International Medical Device Regulators Forum.
Aktualisierungen der Tabellen
Aufgrund der Besonderheiten der Medizinprodukteindustrie und der Einführung neuer Technologien, Materialien, Konstruktionen, Verfahren usw. ist davon auszugehen, dass die Terminologie für Medizinprodukte und zugehörige Komponenten aktualisiert werden muss, um den technischen Fortschritt zu berücksichtigen. Aus diesem Grund ist eine regelmäßige Überprüfung und Pflege der Terminologien und Codes erforderlich, um gegebenenfalls Begriffe hinzuzufügen, zu ändern oder zu streichen. Wenn Begriffe überflüssig werden, werden diese veralteten Begriffe und die entsprechenden Codes nicht gelöscht, sondern als „inaktiv“ gekennzeichnet. Diese obsoleten Begriffe stehen nur noch als Referenz zur Verfügung, können aber nicht mehr ausgewählt werden. Es gibt zwei Möglichkeiten, wie mit inaktiven Codes verfahren werden kann:
1) Umkodierung – Alle Codes im internen System anpassen
2) Übergangsdatum setzen – Zeitpunkt ab dem neu codiert wird
Ersteres ist eher nicht zu empfehlen. Die Umkodierung ist mit erheblichem Aufwand verbunden und kann durchaus zu zusätzlichen Meldungen an die Regulierungsbehörden führen. Bei der Einführung eines Übergangsdatums müssen die Auswertungen ggf. an die neuen Codierungen angepasst werden, verursachen aber ansonsten keinen Mehraufwand.
Die Einreichung von Änderungsanträgen ist bis zum 1. September eines Jahres möglich. Das Update wird Im März des Folgejahres veröffentlicht.
Alle Änderungen sind in Anhang B: IMDRF terminologies for categorized Adverse Event Reporting (AER) – Change Log entnommen angegeben. Änderungsanträge können nicht von Einzelpersonen gestellt werden, sondern laufen über national zuständige Behörden oder Interessensvertreter. Weitere Informationen können der folgenden Webpage des IMDRF entnommen werden IMDRF Adverse Event Terminology Maintenance | International Medical Device Regulators Forum.
Weitere Erläuterungen zu den Anhängen A-F
Begriffe/Codes für Probleme mit Medizinprodukten (Annex A – A XX|XX|XX):
Diese Begriffe ermöglichen es, die auf der Produktebene aufgetretenen Probleme durch Beobachtungen zu erfassen, ohne jedoch die möglichen Gründe oder Ursachen für die beobachteten Probleme oder Ausfälle zu beschreiben. Anhang A enthält eine umfassende, hierarchisch gegliederte Liste von Begriffen und Codes für Probleme mit Medizinprodukten. Die Begriffe und Codes auf dieser Ebene sind beispielhaft in Abb. 5 dargestellt.
Begriffe/Codes für die Ursachenermittlung (Annex B-D):
Mit diesen Begriffen werden die Art der durchgeführten Untersuchung, die Ergebnisse der Untersuchung und die Schlussfolgerung der Ursachenermittlung aus der Untersuchung erfasst.
Begriffe/Codes für die Art der Untersuchung (Annex B – B XX): Anhang B gibt an, was untersucht wurde um die Art des Vorkommnisses zu ermitteln. In diesem Anhang gibt es nur Begriffe für Level 1. Werden zum Beispiel die Produktionsaufzeichnungen untersucht, kann als Begriff „Analysis of Production Records“ – B14 gewählt werden.
Begriffe/Codes für Untersuchungsergebnisse (Annex C – C XX|XX|XX): Anhang C enthält die Ergebnisse der spezifischen Untersuchung, die der Schlüssel zur Ermittlung der Ursache ist. Dieser Anhang ist wie auch Anhang A hierarchisch gegliedert. Wenn man das oben genannte Beispiel für Anhang B (B14) weiter betrachtet, könnte das Ergebnis der Untersuchung sein, dass es Probleme während des Herstellungsprozesses gab, z.B. Montageprobleme (Assembly Problem Identified – C1601).
Begriffe/Codes für Schlussfolgerungen der Untersuchung (Annex D – D XX|XX): Anhang D enthält die Schlussfolgerungen aus der Untersuchung. In den Schlussfolgerungen wird die Ursache für das jeweilige unerwünschte Ereignis angegeben. Auch dieser Anhang ist hierarchisch gegliedert, jedoch nur in zwei Level. Eine mögliche Schlussfolgerung könnte hierbei sein, dass das Vorkommnis auf ein Problem während des Herstellungsprozesses zurückzuführen ist (Manufacturing Deficiency – D0103) und es könnte auch durch unzureichendes Training verursacht worden sein (Cause Traced to Training – D08).
Begriffe/Codes für gesundheitliche Auswirkungen (Annex E und F): Mit diesen Begriffen werden die beobachteten Anzeichen und Symptome sowie die Ergebnisse im Zusammenhang mit dem unerwünschten Ereignis eines Medizinprodukts erfasst. Es werden keine diagnostischen Merkmale verwendet. Anhang E enthält eine Liste klinischer Anzeichen, Symptome und Zustände, die detailliert genug ist, um die gesundheitlichen Auswirkungen für die Meldung von unerwünschten Ereignissen oder Vorfällen im Zusammenhang mit Medizinprodukten zu erfassen. Gleichzeitig ist sie allgemein genug, um den Aufbau weiterer umfassender Terminologie-Systeme zu vermeiden. Anhang F enthält eine Liste möglicher Folgen und Auswirkungen des Vorkommnisses. Die Begriffe aus diesen beiden Anhängen ergeben zusammen eine Beschreibung, die sowohl die klinische Beobachtung als auch die Auswirkungen auf die betroffene Person umfasst.
Begriffe/Codes für klinische Anzeichen, Symptome und Zustände (Annex E – E XX|XX|XX): Anhang E enthält eine Terminologie zur Beschreibung des beobachteten Zustands der betroffenen Personen im Zusammenhang mit dem Vorkommnis eines Medizinprodukts. Diese Begriffe sollten nicht zur Beschreibung von Anzeichen, Symptomen und Zuständen verwendet werden, die bereits vor dem Vorkommnis bestanden. Durch die enge Zusammenarbeit zwischen IMDRF und MedDRA sind diese Begriffe eng an eine Untergruppe der MedDRA-Begriffe angelehnt. Eine Zuordnung der IMDRF Codes zu den MedDRA-Begriffen ist in der Tabelle in Anhang E zu finden. Dieser Anhang ist in Kategorien nach Organsystemen und physiologischen Problemen kategorisiert. Einige Begriffe erscheinen in mehr als einer Kategorie, um das Auffinden des richtigen Begriffs zu erleichtern. In diesen Fällen wird jedem sich wiederholenden Begriff nur ein eindeutiger Code auf der Grundlage seiner primären Kategorie zugewiesen.
Begriffe/Codes für klinische Anzeichen, Symptome und Zustände (Annex E – E XX|XX|XX): Anhang E enthält eine Terminologie zur Beschreibung des beobachteten Zustands der betroffenen Personen im Zusammenhang mit dem Vorkommnis eines Medizinprodukts. Diese Begriffe sollten nicht zur Beschreibung von Anzeichen, Symptomen und Zuständen verwendet werden, die bereits vor dem Vorkommnis bestanden. Durch die enge Zusammenarbeit zwischen IMDRF und MedDRA sind diese Begriffe eng an eine Untergruppe der MedDRA-Begriffe angelehnt. Eine Zuordnung der IMDRF Codes zu den MedDRA-Begriffen ist in der Tabelle in Anhang E zu finden. Dieser Anhang ist in Kategorien nach Organsystemen und physiologischen Problemen kategorisiert. Einige Begriffe erscheinen in mehr als einer Kategorie, um das Auffinden des richtigen Begriffs zu erleichtern. In diesen Fällen wird jedem sich wiederholenden Begriff nur ein eindeutiger Code auf der Grundlage seiner primären Kategorie zugewiesen.
Begriffe/Codes für klinische Anzeichen, Symptome und Zustände (Annex E – E XX|XX|XX): Anhang E enthält eine Terminologie zur Beschreibung des beobachteten Zustands der betroffenen Personen im Zusammenhang mit dem Vorkommnis eines Medizinprodukts. Diese Begriffe sollten nicht zur Beschreibung von Anzeichen, Symptomen und Zuständen verwendet werden, die bereits vor dem Vorkommnis bestanden. Durch die enge Zusammenarbeit zwischen IMDRF und MedDRA sind diese Begriffe eng an eine Untergruppe der MedDRA-Begriffe angelehnt. Eine Zuordnung der IMDRF Codes zu den MedDRA-Begriffen ist in der Tabelle in Anhang E zu finden. Dieser Anhang ist in Kategorien nach Organsystemen und physiologischen Problemen kategorisiert. Einige Begriffe erscheinen in mehr als einer Kategorie, um das Auffinden des richtigen Begriffs zu erleichtern. In diesen Fällen wird jedem sich wiederholenden Begriff nur ein eindeutiger Code auf der Grundlage seiner primären Kategorie zugewiesen.
Tipps zur Anwendung der IMDRF-Tabellen
Die Anwendung der IMDRF-Tabellen zur Dokumentation von Vorkommnissen mag auf den ersten Blick komplex erscheinen. Bei sieben Tabellen und einer Vielzahl von Begriffen kann man leicht den Überblick verlieren. Mit einigen gezielten Ansätzen kann der Prozess jedoch erheblich vereinfacht werden. Im Folgenden werden einige Tipps gegeben, wie Sie die Tabellen effizient genutzt werden können.
Überblick verschaffen und Sortieren
Der erste Schritt zur erfolgreichen Anwendung der Tabellen besteht darin, sich mit ihrem Aufbau und Inhalt vertraut zu machen. Es ist unerlässlich, den Inhalt der Tabellen vollständig durchzugehen, um sich einen Überblick zu verschaffen. Besonders hilfreich ist es, die Begriffe in den Tabellen vorab anhand des eigenen Produktes zu sortieren. So können offensichtlich nicht relevante Codes frühzeitig ausgeschlossen werden. Ein Beispiel: Für ein klassisches Infusionsbesteck ohne elektronische Komponenten können Begriffe oder Codes ausgeschlossen werden, die im Zusammenhang mit Elektroschocks stehen.
Anwendung der Suchfunktion: Synonyme und alternative Begriffe nutzen
Wenn Ihnen ein Vorfall gemeldet wird, enthält diese Meldung im besten Fall bereits einige wichtige Informationen wie:
- Was ist passiert?
- Wer und welche Produkte waren bei dem Vorfall beteiligt?
- Ist jemand zu Schaden gekommen?
- Welche Auswirkungen hatte das Ereignis auf die betroffene(n) Person(en)?
Auf der Grundlage dieser Informationen ist es möglich und in einigen Fällen vorteilhaft, die Suchfunktion zu verwenden. Bei der Suche nach passenden Codes ist es hilfreich, sich nicht strikt an die genannten Begriffe zu halten. Stattdessen können Synonyme oder alternative Formulierungen in Betracht gezogen werden.
Detaillierte Beschreibung durch präzise Codes
Für die Dokumentation eines Vorkommnisses gilt: Je detaillierter die Beschreibung, desto besser. Wann immer möglich, sollten Level-3-Codes verwendet werden, da diese den höchsten Detaillierungsgrad bieten. Wenn nicht genügend Informationen verfügbar sind, können auch Level-2- oder Level-1-Codes verwendet werden. In einigen Fällen kann es sinnvoll sein, mehrere Codes innerhalb desselben Anhangs anzugeben, um das Ereignis umfassender zu beschreiben.
Keine passenden Begriffe oder unzureichende Informationen
Wenn weder ein passender Begriff noch ausreichende Informationen vorhanden sind und auch die Level-1-Begriffe nicht angewendet werden können, bieten die Tabellen dennoch Lösungsmöglichkeiten. Für solche Fälle gibt es spezifische Codes wie z.B.:

Diese Codes ermöglichen es, auch unvollständige oder nicht eindeutig zuzuordnende Vorkommnisse adäquat zu dokumentieren.
Standardisierte Code Sets für wiederkehrende Fälle
Bei häufig auftretenden Vorkommnissen kann die Dokumentation durch die Verwendung von festen Codesets wesentlich effizienter gestaltet werden. Das Festlegen solcher standardisierter Codes gewährleistet eine einheitliche und konsistente Dokumentation, was nicht nur Zeit spart, sondern auch die interne Auswertung der Daten vereinfacht.
Besonderheiten der einzelnen Anhänge
Annex E: Dieser Anhang enthält besonders spezifische Begriffe auf Level 3. Bei Unsicherheiten in der Zuordnung, ist es ratsam, die entsprechende Fachkompetenz hinzuzuziehen, um die richtigen Begriffe auszuwählen. Ein präziser Code bringt Mehrwert und erhöht die Aussagekraft der Dokumentation.
Annex G: Insbesondere im Annex G empfiehlt es sich, die Suchfunktion zu nutzen, um gezielt nach relevanten Begriffen oder Komponenten zu suchen. Gerade bei komplexeren Produkten kann dies den Prozess erheblich beschleunigen.
Anwendungsbeispiel
Das folgende Fallbeispiel soll die Anwendung der IMDRF-Codes veranschaulichen und basiert auf einem fiktiven Szenario. Die dargestellte Meldung ist bewusst sehr ausführlich beschrieben, um möglichst viele Informationen zu vermitteln, anhand derer die zutreffende Codes auswählt werden können – in der Realität sind solche Meldungen meist deutlich kürzer und Sie müssen die entsprechenden Informationen meist erst anfordern.
Die aufgeführten Codes stellen beispielhafte Möglichkeiten dar, die je nach durchgeführter Ursachenuntersuchung (Cause Investigation) und den daraus gewonnenen Erkenntnissen angewendet werden können. Abhängig von den spezifischen Umständen des Falles können auch andere IMDRF-Codes anwendbar sein. Das Fallbeispiel soll dazu anregen, über die vielfältigen Anwendungsmöglichkeiten der Tabellen nachzudenken und für individuelle Szenarien eine geeignete Auswahl zu treffen.

Basierend auf dem beschriebenen Vorfall mit dem elektronischen Blutdruckmessgerät und unter Verwendung der IMDRF-Terminologie für die Meldung von unerwünschten Ereignissen, könnten die entsprechenden Codes für die Anhänge A bis G wie folgt lauten:
Anhang A: Medical Device Problem Terms and Codes
- Code: A1406
- Term: Inflation problem
- Description: Problem associated with the inability of the device to expand or enlarge with the intended inflation agent (e.g. saline or air).
- Begründung: Probleme beim Aufblasen der Manschette, wie z.B. unvollständiges oder übermäßiges Aufblasen.
Anhang B: Cause Investigation – Type of Investigation Terms and Codes
- Code: B01
- Term: Testing of Actual/Suspected Device
- Description: The investigation employed relevant empirical testing of the actual device suspected in the reported adverse event in order to establish their functional and other properties and to identify possible causes for the adverse event. Relevant testing would typically be based on test methods used for evaluating safety and performance as described in the latest relevant standards.
- Begründung: Das tatsächliche Gerät, das vom Ereignis betroffen war, müsste getestet werden, um die Funktionalität und mögliche Ursachen für das Problem (z. B. Mechanik oder Elektronik) zu identifizieren.
- Code: B14
- Term: Analysis of Production Records
- Description: The investigation involved the analysis of relevant production records in view of supporting the identification of possible causes for the adverse event.
- Begründung: Die Produktionsaufzeichnungen sollten überprüft werden, um festzustellen, ob während der Herstellung oder Qualitätskontrolle Probleme aufgetreten sind, die das Ereignis erklären könnten.
- Code: B24
- Term: Event History Log Review
- Description: The investigation involved the analysis of the history log files retrieved from the device to support possible causes for the adverse event, includes device interrogation.
- Begründung: Eine Überprüfung der Verlaufsprotokolle des Geräts (sofern vorhanden) könnte wichtige Hinweise auf Fehlfunktionen oder Benutzerinteraktionen vor dem Vorfall geben.
Anhang C: Cause Investigation – Investigation Findings Terms and Codes
- Code: C0201
- Term: Electrical/Electronic Component Problem Identified
- Description: The performance of an electrical or electronic component was found to be inadequate.
- Begründung: Ausfall einer Komponente des Geräts, der zum beschriebenen Problem führte.
Anhang D: Cause Investigation – Investigation Conclusion Terms and Codes
- Code: D02
- Term: Cause Traced to Component Failure
- Description: Expected or random component failure without any design or manufacturing issue.
- Begründung: Das Problem mit der Blutdruckmanschette könnte durch den Ausfall einer elektrischen oder mechanischen Komponente verursacht worden sein. Da die Luft nicht entwich, obwohl das Gerät ausgeschaltet war, könnte dies auf eine Fehlfunktion im Ventilsystem oder der Steuerungselektronik hinweisen.
- Code: D0102
- Term: Human Factors Engineering – Device Difficult to Operate
- Description: Problems traced to inappropriate and/or inadequate design of the user interface or usability of the device.
- Begründung: Falls das Gerät keine Möglichkeit bot, den übermäßigen Druck manuell abzulassen oder die Benutzerführung unzureichend war, könnte dies auf eine unzureichende Berücksichtigung menschlicher Faktoren im Design zurückzuführen sein.
- Code: D0105
- Term: Missing or Inadequate Safety Measures
- Description: Problems traced to inadequate design or complete lack of safety features and/or protective measures.
- Begründung: Falls das Gerät keine Sicherheitsmechanismen hatte, um übermäßigen Druck automatisch abzubauen oder einen Notablass zu ermöglichen, wäre dieser Code passend.
- Code: D0108
- Term: Inadequate Software Design
- Description: Cause traced to inadequate or inappropriate design of the device software resulting in device malfunction
- Begründung: Da das Gerät eine Fehlermeldung („E04 – Manschettendruck zu hoch“) anzeigte, aber die Luft trotzdem nicht entwich, könnte eine Softwarefehlfunktion vorliegen, die das Ablassen der Luft blockierte.
Anhang E: Health Effects – Clinical Signs, Symptoms and Conditions Terms and Codes
- Code: E2330
- Term: Pain
- Description: An unpleasant sensory and emotional experience that is associated with actual or potential tissue damage or described in such terms.
- Begründung: Die Patientin verspürte Schmerzen im Arm aufgrund des anhaltenden Drucks der Manschette.
Anhang F: Health Effects – Health Impact Terms and Codes
- Code: F26
- Term: No health consequences or impact
- Description: No apparent harm occurred in relation to the adverse event.
- Begründung: Es traten keine langfristigen gesundheitlichen Folgen für die Patientin auf.
Anhang G: Medical Device Component Terms and Codes
- Code: G02027
- Term: Power Supply
- Definition: Component designed to supply electrical power to a device or system.
- Begründung: Falls das Blutdruckmessgerät eine fehlerhafte Stromversorgung hatte (z. B. Spannungsprobleme), könnte dies dazu geführt haben, dass die Steuerelektronik nicht korrekt funktionierte und die Luft nicht entweichen konnte.
- Code: G02026
- Term: Power Cord
- Definition: A flexible cable designed to connect an electrical device to a power source.
- Begründung: Ein Wackelkontakt oder eine unzureichende Stromzufuhr könnte zu einem unkontrollierten Verhalten des Geräts geführt haben, sodass das Ventil nicht mehr ordnungsgemäß funktionierte.
- Code: G02004
- Term: Cable, Electrical
- Definition: A long, thin, multistranded electrical wire designed to conduct electricity within or between devices.
- Begründung: Falls eine interne Verkabelung defekt war, könnte die Steuerung der Luftfreigabe beeinträchtigt gewesen sein.
- Code: G0203401
- Term: Power Switch
- Definition: A switch designed to regulate the power to a device or a specific function within a device.
- Begründung: Falls das Gerät nicht korrekt ausgeschaltet wurde oder der Schalter defekt war, könnte dies dazu geführt haben, dass die Luftfreigabe nicht mehr funktionierte.
Nachdem Sie die Grundlagen zu IMDRF-Codes kennengelernt haben, können Sie direkt mit der Anwendung starten. Auf dieser Seite finden Sie unsere Web-Applikation AERcodes.





